U NGUYÊN BÀO THẦN KINH ĐỆM
Dịch tễ học
U não tiên phát ác tính vẫn là một thách thức trong y khoa. U nguyên bào thần kinh đệm (còn gọi là u tế bào thần kinh đệm độ IV, u sao bào độ IV) là u não tiên phát phổ biến và ác tính nhất. U nguyên bào thần kinh đệm là hình ảnh thu nhỏ của một nhóm u tế bào thần kinh đệm (glioma). U tế bào thần kinh đệm bao gồm rất nhiều loại u khác nhau, có chung đặc điểm là các tế bào ác tính lan tỏa và thâm nhiễm vào nhu mô não. Theo dữ liệu của tổ chức theo dõi ung thư Mỹ (Cancer Brain Tumor Registry of the United States), glioma chiếm 30% tổng số u não tiên phát và u hệ thần kinh trung ương, và chiếm 80% u não ác tính tiên phát của hệ thần kinh trung ương. U sao bào và u nguyên bào thần kinh đệm chiếm 76% các loại glioma. Tỷ lệ mắc mới của u nguyên bào thần kinh đệm là 3/100 000 người mỗi năm, độ tuổi trung bình là 64 và gặp nhiều nhất ở độ tuổi 65-74, tỷ lệ nam: nữ là 1.5:1.
Đặc điểm hình ảnh
Hình ảnh của u nguyên bào thần kinh đệm trên phim MRI thể hiện những thay đổi vi môi trường điển hình cho quá trình phát triển của u nguyên bào thần kinh đệm. Bao gồm hình ảnh nhiều vùng hoại tử cũng như phù nề và các mạch máu u tân sinh bị dò (leaky tumor vessels), do đó u có hình ảnh bắt thuốc tương phản mạnh ở ngoại vi, và thường đi kèm vùng hoại tử trung tâm không bắt thuốc. Tất cả các yếu tố này kết hợp lại tạo ra những đặc điểm vi môi trường chỉ có ở u nguyên bào thần kinh đệm, và những đặc điểm này cực kỳ tương phản với nhu mô não bình thường khi phân tích về mặt mô học. Trong khi CT scan chỉ là phương tiện chẩn đoán hình ảnh có thể được chỉ định ban đầu để loại sàng lọc khối choán chỗ ở não, MRI sọ não không và có tiêm Gadolinium là xét nghiệm chẩn đoán hình ảnh được lựa chọn trong chẩn đoán u não. U nguyên bào thần kinh đệm và glioma độ cao dễ phân biệt với glioma độ thấp vì chúng thường có hình ảnh cản quang không đồng đều trên phim MRI và phù nề đáng kể quanh u (hình 1). U nguyên bào thần kinh đệm phát triển nhanh và thường có biểu hiện yếu ứng choán chổ, phù nề, xuất huyết, hoại tử và biểu hiện của tăng áp nội sọ. U nguyên bào thần kinh đệm khác với ap-xe não ở đặc điểm ap-xe não thường có khuếch tán bị giới hạn rõ rệt trên chuỗi xung DWI. Chuỗi xung FLAIR có thể giúp xác định mức độ phù nề quanh u.
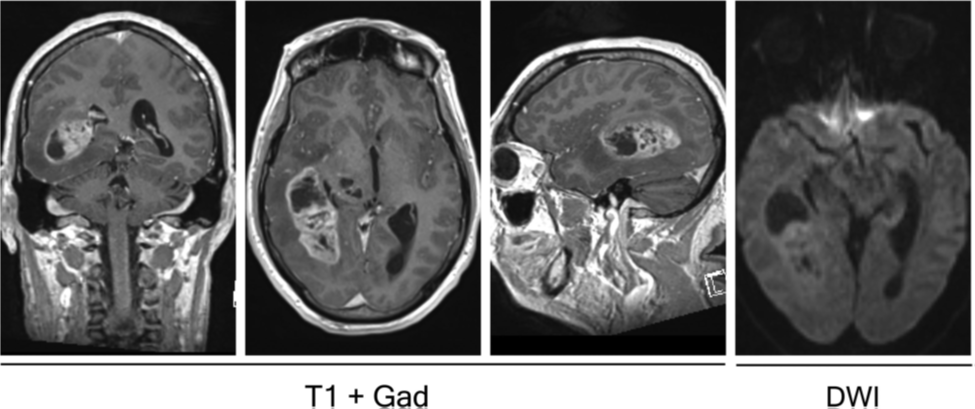
Hình 1. Phim MRI cho thấy khối u nguyên bào thần kinh đệm ở thái dương phải. Chuỗi xung T1 sau tiêm đối quang mặt phẳng coronal, axial, và sagittal (từ trái sang phải) cho thấy tổn thương bắt đối quang không đồng đều và có hiệu ứng choán chổ kèm phù nề, tương thích với hình ảnh của u nguyên bào thần kinh đệm. Hình ảnh ngoài cùng bên phải là ở chuỗi xung khuếch tán (DWI) cho thấy không có sự giới hạn khuếch tán, điều này giúp loại trừ ap-xe não.
Phim MRI chức năng đóng vai trò quan trọng khi làm xét nghiệm cho bệnh nhân bị u nguyên bào thần kinh đệm, mục đích để xác định các vùng vỏ não chức năng quan trọng và mối tương quan của chúng với u (hình 2). Thông tin về mối liên quan này sẽ giúp quá trình bóc u được hiệu quả và an toàn. Ở hình 2, bệnh nhân có khối u nguyên bào thần kinh đệm lớn ở thái dương trái. MRI chức năng cho thấy vùng ngôn ngữ tiếp nhận (vùng Wernicke) nằm ngay cạnh khối u ở bờ sau của thùy thái dương trên.
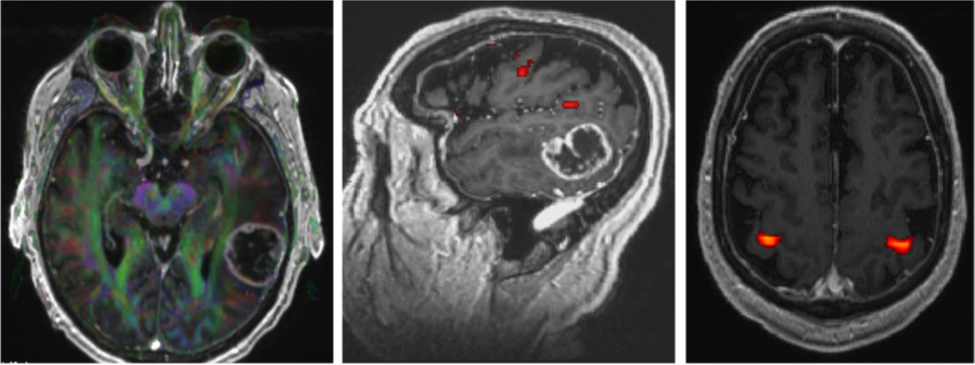
Hình 2. MRI chức năng xác định các dãi chất trắng (hình bên trái), vùng ngôn ngữ (hình giữa) và vùng vận động của tay (hình bên phải).
Phương pháp tốt nhất cho bệnh nhân này là phẫu thuật mở sọ tỉnh (awake craniotomy) để xác định vùng vỏ não phụ trách chức năng nói, nhờ đó phẫu thuật viên có thể lấy bỏ được tối đa khối u và giảm thiểu nguy cơ bị rối loạn ngôn ngữ vĩnh viễn. Trong quá trình phẫu thuật tỉnh, bệnh nhân được yêu cầu thực hiện một loạt các nhiệm vụ thần kinh liên quan đến lời nói trong khi bác sĩ phẫu thuật kích thích não bằng một đầu dò điện. Khu vực phụ trách lời nói quan trọng được xác định sẽ không bị cắt bỏ, ngay cả khi khối u thâm nhiễm vào các khu vực này.
Bất thường về gen
Hầu hết các u nguyên bào thần kinh đệm dường như xuất hiện rải rác, không có mối liên hệ cơ học với các yếu tố môi trường hoặc hành vi, chẳng hạn như hút thuốc lá hoặc điện từ trường. U nguyên bào thần kinh đệm hoặc phát sinh ngay từ đầu (de novo) (u nguyên bào thần kinh đệm tiên phát) hoặc tiến triển từ u tế bào hình sao độ thấp hơn (u nguyên bào thần kinh đệm thứ cấp) thông qua nhiều lần biến đổi gen. Khuếch đại đường truyền tín hiệu của yếu tố tăng trưởng có nguồn gốc từ biểu bì và tiểu cầu, đột biến p53, thay đổi đường dẫn của u nguyên bào võng mạc, và các thay đổi về nhiễm sắc thể số 10, bao gồm cả đột biến PTEN (phosphatidylinositol 3-phosphatase), là những thay đổi ở mức độ phân tử phổ biến nhất liên quan đến sự tiến triển của u tế bào hình sao độ thấp trở thành u nguyên bào thần kinh đệm. Những thay đổi trong một số con đường dẫn truyền tín hiệu nội bào dẫn đến mất sự lão hóa và các điểm kiểm tra chu kỳ tế bào góp phần tạo nên tính đa hình và kiểu nhân không đồng nhất (karyotypic heterogeneity) trong tế bào u nguyên bào thần kinh đệm. Tình trạng methyl hóa gen O6-methylguanine DNA methyltransferase (MGMT) và đột biến gen isocitrate dehydrogenase (IDH) là 2 khám phá di truyền gần đây có ý nghĩa tiên lượng lâm sàng ở bệnh nhân u nguyên bào thần kinh đệm. Gen MGMT mã hóa một loại enzyme có nhiệm vụ sửa chữa DNA bị hỏng. Bệnh nhân với tình trạng tăng methyl hóa MGMT bị giảm khả năng sửa chữa DNA, và nghiên cứu cho thấy những bệnh nhân này đáp ứng với trị liệu alkyl hóa, chẳng hạn như temozolimide. Ngoài ra, các đột biến IDH được tìm thấy trội hơn hẳn ở u nguyên bào thần kinh đệm thứ phát và trong phần lớn các u thần kinh đệm độ thấp. Đột biến IDH có liên quan đến việc cải thiện thời gian sống ở bệnh nhân bị u thần kinh đệm thông qua một cơ chế mà cho đến nay vẫn chưa được hiểu rõ.
Biểu hiện lâm sàng
U nguyên bào thần kinh đệm có thể xuất hiện tiên phát hoặc thứ phát (tiến triển từ u tế bào hình sao độ thấp), sau khi trải qua nhiều lần biến đổi gen như đã đề cập ở trên. Bệnh nhân u nguyên bào thần kinh đệm thứ phát thường có một quá trình lâm sàng bắt đầu từ độ tuổi 20 đến dưới 40, ban đầu là u thần kinh đệm độ thấp (độ 2) tiến triển theo thời gian thành u thần kinh đệm độ cao (độ 3 hoặc độ 4). Bệnh nhân u nguyên bào thần kinh đệm tiên phát thường xuất hiện muộn hơn, ở độ tuổi 50 đến dưới 80 tuổi và không có tiền sử u trước đó. Các triệu chứng thường tiến triển trong một khoảng thời gian ngắn và bệnh nhânvào viện với khối u lớn tăng tín hiệu trên MRI. Do tốc độ tăng sinh lớn, các mạch máu không đáp ứng kịp tốc độ tăng trưởng của u nguyên bào thần kinh đệm, dẫn đến hình thành nhiều ổ hoại tử và thiếu oxy, nên kích thích sự tăng sinh mạch. Không may là các mạch máu tân sinh thường khiếm khuyết, có nhiều shunt nối với nhau và hàng rào máu não bị rò rỉ, dẫn đến phù não khu trú và hiệu ứng choán chổ quanh u. Các bệnh nhân thường có biểu hiện giống nhau là tăng áp nội sọ dưới dạng đau toàn đầu, đau tăng lên khi ho hoặc khi nằm. Bệnh nhânthường sẽ xuất hiện các triệu chứng khác bao gồm buồn nôn và nôn, mờ mắt, phù gai thị và thậm chí có thể liệt các dây thần kinh sọ, và có khiếm khuyết về vận động và cảm giác. Nếu hiệu ứng choán chổ đủ lớn và đường giữa bị đẩy lệch nhiều, trạng thái tâm thần và sự tỉnh táo của bệnh nhân có thể bị ảnh hưởng. Ngoài ra, khi các khối u thâm nhiễm các cấu trúc chức năng ở não bộ, thị giác và lời nói có thể bị ảnh hưởng ngay từ đầu.
Mức độ bóc u
Nghiên cứu cho thấy mức độ cắt bỏ khối u có ảnh hưởng thời gian sống của bệnh nhân, khối u được lấy bỏ càng nhiều thì thời gian sống sau mổ càng được kéo dài. U tế bào thần kinh đệm nổi tiếng về tính xâm lấn và thâm nhiễm nhu mô não bình thường, nên việc cắt bỏ hoàn toàn khối u về cơ bản là không thực hiện được. Tiên lượng của u nguyên bào thần kinh đệm rất xấu, cho dù phẫu thuật cắt bỏ rộng rãi khối u, kết hợp xạ và hóa trị tối ưu sau mổ thì thời gian sống sót trung bình của bệnh nhân u nguyên bào thần kinh đệm hiện nay vẫn chỉ khoảng 15 tháng. Phần lớn bệnh nhân u nguyên bào thần kinh đệm tử vong trong vòng 2 năm và gần như tất cả bệnh nhân sống sót sau 2 năm đều tử vong trước 5 năm. Mức độ cắt bỏ u nguyên bào thần kinh đệm dường như tương quan với tỷ lệ sống sót và kết quả điều trị của bệnh nhân nhưng kết luận này phần lớn dựa trên các nghiên cứu hồi cứu, vốn có các sai số và các yếu tố gây nhiễu. Vẫn còn thiếu các nghiên cứu đối chứng ngẫu nhiên để kiểm chứng về kết luận này do thiếu đối trọng lâm sàng để thực hiện. Các số liệu về thời gian sống sót trên lâm sàng và dữ liệu nghiên cứu khoa học cơ bản cho thấy loại ung thư này có đặc tính sinh học rất ác tính, nên một số chuyên gia đã chỉ ra rất chi tiết rằng “phẫu thuật bóc u rộng rãi hơn không cải thiện đáng kể thời gian sống sót bệnh nhân”. Mặc dù những tiến bộ về chẩn đoán hình ảnh, kỹ thuật phẫu thuật, thuốc và hiểu biết ở mức độ phân tử của căn bệnh này đã đem lại những cải thiện khiêm tốn về kết quả điều trị trong 3 thập kỷ qua, vẫn còn thiếu những đột phá đáng kể trong điều trị. Những hiểu biết sâu sắc hơn về quá trình bệnh lý và phương pháp điều trị đích ở mức độ phân tử hợp lý hơn trong tương lai có thể đem lại bước đột phá trong điều trị bệnh lý này.
Phẫu thuật và điều trị bằng thuốc
Bệnh nhân thường xuất hiện triệu chứng cấp tính với khối u lớn, phù não quanh u và có hiệu ứng choán chổ và cần phải nhập viện. Điều trị giảm nhẹ triệu chứng bằng steroid và làm các xét nghiệm về ung thư để xác định xem tổn thương là u não nguyên phát hay di căn. Dexamethasone thường được sử dụng để điều trị phù não, thuốc này thường sẽ cải thiện các triệu chứng thần kinh. Nếu bệnh nhâncó biểu hiện co giật, cần cho thuốc chống động kinh (AED). Ở đây, quyết định phẫu thuật được đưa ra. Mục tiêu của phẫu thuật là cắt bỏ tối đa khối u và hạn chế biến chứng thần kinh. Bệnh nhân với khối u nằm sâu hoặc liên quan đến cấu trúc não chức năng có thể không phải là ứng cử viên cho phẫu thuật bóc u rộng rãi mà thay vào đó là sinh thiết để chẩn đoán và làm các xét nghiệm phân tử tổ chức u. Bệnh nhân với khối u có thể tiếp cận được bằng phẫu thuật sẽ được cắt bỏ u tối đa. Bệnh nhân có thể được giảm liều steroid dần rồi ngưng hẳn hoặc giảm dần về liều cơ bản dựa trên mức độ còn lại của khối u, độ phù nề và sự ưa thích của bác sĩ ung thư thần kinh và bác sĩ xạ trị ung thư. Phác đồ điều trị sau phẫu thuật được dựa trên một nghiên cứu đối chứng ngẫu nhiên mà kết quả cho thấy cải thiện tỷ lệ sống sót sau 2 năm và thường được gọi là phác đồ Stupp:
-Xạ trị:
+Tổng liều: 60 Gy
+2 Gy mỗi ngày (thứ hai đến thứ 6) trong 6 tuần
-Tezolomide:
+Trong quá trình xạ trị: 75 mg /m2 diện tích da cơ thể/ ngày, 7 ngày/ tuần
+Sau xạ trị (liều bổ sung): 6 chu kỳ, bao gồm 150-200 mg/ đơn vị m2 diện tích
da cơ thể trong 5 ngày cho mỗi chu kỳ 28 ngày.
Mục tiêu phẫu thuật cho bệnh nhân u nguyên bào thần kinh đệm là (1) có được tổ chức mô để chẩn đoán mô bệnh học (2) giải ép, và (3) cắt bỏ khối u để giảm gánh nặng tế bào u (cytoreduction). Bóc u toàn bộ và hạn chế tối đa khiếm khuyết chức năng sau mổ thường là mục tiêu của cuộc mổ.
Tích hợp theo dõi thần kinh với phẫu thuật não tỉnh là những tiến bộ quan trọng cho phép phẫu thuật viên bóc được u tối đa và tránh gây tổn thương vùng vỏ não chức năng và các cấu trúc quan trọng. Gần đây, việc sử dụng thuốc nhuộm, ví dụ axit 5-aminolevulinic, là chất được tổ chức u ưu tiên bắt giữ đã giúp phẫu thuật viên xác định ranh giới thâm nhiễm của khối u để bóc u tối đa. Tuy nhiên, vẫn cần có thêm các thử nghiệm lâm sàng để xác định hiệu quả của các tác nhân này.
Các điểm cần ghi nhớ
-U nguyên bào thần kinh đệm là u não nguyên phát ác tính phổ biến nhất và có tiên lượng xấu.
-Chẩn đoán phân biệt đối với các tổn thương có bắt thuốc đối quang ở ngoại vi là rất rộng. MRI có thể giúp phân biệt u nguyên bào thần kinh đệm với các bệnh lý khác.
-Điều trị hiện tại cho u nguyên bào thần kinh đệm là cắt bỏ tối đa u một cách an toàn, sau đó là xạ trị và hóa trị.
-Mục tiêu của phẫu thuật cho bất kỳ bệnh nhân u nguyên bào thần kinh đệm nào là (1) lấy tổ chức u để chẩn đoán mô bệnh học và nghiên cứu di truyền / phân tử (2) giải phóng não bộ khỏi hiệu ứng choán chỗ, và (3) giảm gánh nặng tế bào của khối u.
BS. Trương Văn Trí biên dịch
Nguồn:
- J.Bradley Elder, Essential neurosurgery for medical students- Tumor- Operative neurosurgery, volume 17, number 2, S119-S124, 2019
- Mark S. Greenberg, “Primary Tumor of the Nervous and Related System”, Handbook of Neurosurgery 9th edition, Thieme Medical Publishers, NewYork, NY, pp.591-735, 2020





